Kardioplegija
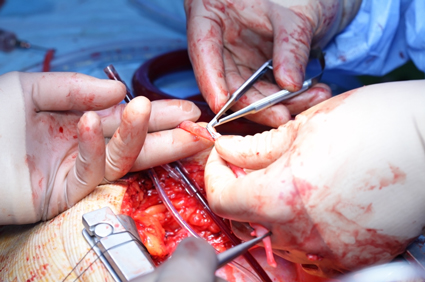
Kardioplegična otopina koristi se kod operacija srca u ekstrakorporalnoj cirkulaciji radi zaustavljanja rada srca (prekida električnih i mehaničkih aktivnosti) i zaštite miokarda od ishemične lezije. Prekid krvotoka u koronarnim arterijama dovodi do ishemije srčanog mišića, pa se za njegovu protekciju pri zaustavljanju srca i cirkulacije u miokardu daje infuzija otopine kalija (kardioplegične otopine) u koronarne arterije.
Prva operacija na otvorenom srcu učinjena je 1952.g. u Minneapolisu kada su Lewis i Taufic zatvorili defekt interatrijskog septuma. Miokard su zaštitili umjerenom sistemskom hipotermijom (30°C). Operativno vrijeme bilo je ograničeno na 10 minuta.
1955. Melrose i Bentall uveli su tehniku induciranog elektivnog srčanog aresta injicirajući 2.5% otopinu kalij-citrata u korijen aorte i time ustanovili metodu današnje kardioplegije Ova tehnika je bila napuštena zbog velike incidencije fibroze miokarda uzrokovane visokim koncentracijama kalija. Tako je kardioplegija bila zapostavljena više od deset godina (inače, izraz kardioplegija prvi put upotrebljava 1955. Lam).
1960-te i 70-te godine su bile obilježene raznolikošću metoda protekcije miokarda - koronarna perfuzija, Cooley-ev normotermični ishemični arest, intermitentni cross clamping aorte i Sumway-eva topična hipotermija.
1973. Gay i Ebert su modificirali Melroseov koncept induciranog aresta smanjujući koncentraciju kalija ostvarivši puno bolje rezultate. To je urodilo sve većom koliničkom primjenom, te je kasnih 70-tih godina kardioplegični arest postao opće prihvaćena metoda u svijetu.
1979. Buckberg koristi krv kao sredstvo (medij) za prijenos kalija u koronarne arterije.
1982. Menasche, koristeći se radom Lillehei-a iz 1956. uveo je retrogradnu perfuziju kardioplegične otopine koja omogućuje kontinuirani zahvat, bez prekida radi ponovnih davanja kardioplegije (kao kod anterogradne metode), perfuziju područja distalno od stenoze i smanjuje rizik lezije koronarnih ostija.
1991. Lichtenstein i sur. razvili su novi pristup davanja krvne kardioplegije u normoteriji (37°C).
Principi kardioplegije
Nagli arest srca događa se zbog infuzije kalij-klorida. Medij može biti kristaloidni (kristaloidna kardioplegija) ili krv iz aparata za ekstrakorporalnu cirkulaciju koja osigurava krv i prirodne pufere (krvava kardioplegija).
Neke studije su pokazale da krvava kardioplegija ima prednost pred kristaloidnom u postoperativnom tijeku u smislu poboljšanja sistoličke i dijastoličke funkcije srca. U pacijenata s nestabilnom anginom pektoris korištenje krvave kardioplegije u toku operativnog zahvata značajno je smanjilo incidenciju perioperativnog infarkta miokarda, sindroma niskog minutnog volumena i operativni mortalitet.
Zaustavljanjem srca, potreba miokarda za kisikom se smanjuje za skoro 90%.
Kardioplegija se može davati u hipotermiji (umjerenoj 28-32°C ili dubokoj 18-20°C) ili u normotermiji, pri kojoj enzimatski i stanični reparacijski procesi bolje djeluju. U tom slučaju govorimo o toploj kardioplegiji. U normotermiji kardioplegija mora biti kontinuirana ili s vrlo kratkim prekidima zbog sklonosti srca prema uspostavljanju električne aktivnosti.
Normotermična krvava kardioplegija značajno smanjuje perioperativni infarkt miokarda i potrebu za intraaortalnom balon pumpom. Nadalje, smanjuje značajno smanjuje incidenciju sindroma niskog minutnog volumena, ali nema većih razlika u incidenciji preioperativnog infarkta miokarda i smrtnosti. Kod tehnike parcijalnog klemanja aorte, sistemska normotermija može povećati rizik cerebralne ishemije, pa se tada preferira hipotermijska kardioplegija.
Otopina se može davati anterogradno u korijen aorte i ušća obje koronarne arterije ili retrogradno kroz koronarni sinus.
Kod anterogradne tehnike, nakon klemanja aorte daje se inicijalna doza kardioplegične otopine. Daljnje intermitentne doze kardioplegije daju se nakon šivanja svake distalne anastomoze (kod koronarne kirurgije). Moguće je i kontinuirano anterogradno davanje otopine, no njezin protok otežava vizualizaciju operacijskog polja. Anterogradni način može biti kompromitiran u slučaju teške stenoze koronarnih arterija (posebno proksimalnog dijela), te aortnom regurgitacijom (davanje direktno u koronarna ostija). Kod operacija mitralne valvule, anterogradno davanje kardioplegije zahtijeva prekid kirurških aktivnosti na valvuli radi davanja pune doze otopine.
Retrogradna kardioplegija se koristi posebice u slučajevima teških proksimalnih koronarnih stenoza. Ipak, primjećeno je kod ovakvog načina davanja slabija perfuzija desnog ventrikla, kao i manja kapilarna perfuzija lijevog ventrikla, nego kod anterogradnog načina davanja. Najčešće se retrogradna kardioplegija daje kroz desni atrij u koronarni sinus. Normotermična retrogradna kardioplegija mora se davati kontinuirano da bi se izbjegla ishemija miokarda. Retrogradni način idealan je kod operacija na aortnoj valvuli.
Moguća je i kombinacija ova dva načina: anterogradno/retrogradna kardioplegija, koja koristi najbolje strane i jednog i drugog, ovisno o prirodi bolesti i operativnom nalazu. Ovakva kombinacija osigurava najbolju distribuciju kardioplegije.
Kardioplegičnoj otopini se dodaju različiti aditivi poput glutamata, aspartata, antioksidansa, adenozina i sl. radi poboljšanja protekcije miokarda.
Otopina glukoze i inzulina (l965. Sodi-Pollares) povećava metaboličke rezerve miokarda povisujući nivo srčanog glikogena. Time se smanjuje incidencija aritmija, sindroma niskog minutnog volumena i perioperativnog infarkta.
Glutamat-aspartatom obogaćena kardioplegična otopina pokazala se korisnom u pacijenata s nestabilnom anginom, te visokorizičnih pacijenata u kardiogenom šoku.
Bez obzira na sastav otopine, ujednačena i kvalitetna raspodjela nužna je za optimalnu perioperativnu protekciju miokarda.
Literatura:
- Kirklin JW, Barrat-Boyes BG. Cardiac surgery. New York: Churchill Livingstone; 1993: 141-149.
- Bojar RM. Manual of perioperative care in cardiac surgery. 3rd Edition. Blackwell Science; 1999:102-106.
- Kay PH. Techniques in extracorporeal circulation. 3rd Edition. Butterworth-Heinemann Ltd; 1993: 88-119.
- Brodie JE, Johnson RB. The manual of clinic perfusion. Glendale Medical Corporation; 1994: 49-55.
- Melrose DG, Dreyer B, Bentall HH, Baker JBE: Elective cardiac arrest. Lancet 1955; 2: 21.
- Helmsworth JA, Kaplan S, Clark LC, et al: Myocardial injury associated with asystole induced with potassium citrate. Ann Surg 1959; 149: 200.
- Gay WA: Potassium induced cardioplegia. Ann Thorac Surg 1975; 20: 95.
- Feindel CM, Tait GA, Wilson G: Multidose blood versus crystalloid cardioplegia: Comparison by quantitative assessment of irreversible myocardial injury. J Thorac Cardiovasc Surg 1984; 87: 585.
- Christakis GT, Fremes SE, Weisel RD, et al: Reducing the risk of urgent revascularization for unstable angina: A randomized clinical trial. J Vasc Surg 1986; 3: 764.
- Partington MT, Acar C, Buckberg GD, et al: Studies of retrograde cardioplegia: I. Capillary blood flow distribution to myocardium supplied by open and occluded arteries. J Thorac Cardiovasc Surg 1989; 97: 605.
- Salerno TA, Houck JP, Barrozo CAM, et al: Retrograde continuous warm blood cardioplegia: A new concept in myocardial protection. Ann Thorac Surg 1992; 51: 245.
- Hayashida N, Weisel RD, Shirai T, et al: Tepid antegrade and retrograde cardioplegia. Ann Thorac Surg 1995; 59: 723.
- Svedgeholm R, Huljebrant I, Hakanson E, Vanhanen I: Glutamate and high-dose glucose-insulin-potassium (GIK) in the treatment of severe cardiac failure after cardiac operations. Ann Thorac Surg 1995; 59: S23.
Zadnja izmjena: 31.08.2019.